

植物源外泌体样纳米囊泡(PELNVs)的制备工艺近年涌现了不少创新,主要集中在如何更高效、更智能地获取和利用这些天然的纳米载体。
创新方向 | 核心创新工艺 | 主要优势 | 应用案例 |
提取方法创新 | 酶解法结合新型纯化技术(如水平电泳透析) | 提高提取效率与囊泡完整性,更好地保留生物活性(如蛋白质、miRNA) | 牡丹花瓣纳米囊泡,用于减少紫外辐照引起的细胞损伤 |
载体功能化创新
| 稳定性修饰与靶向修饰结合(如脂肪酸/PEG修饰后连接靶向蛋白Wnt3a) | 增强囊泡稳定性,实现精准靶向递送,提高药物利用率 | 靶向毛囊的载药外泌体,用于治疗白发
|
活性物装载创新 | 优化的超声载药法(精确控制振幅、时间、循环周期) | 工艺简单、环境友好、包埋率高,能显著增强活性物经皮渗透性 | 橄榄叶外泌体包裹羟基积雪草苷,用于抗炎舒缓护肤品 |
来源与工程化创新 | 仿生膜包裹(如红细胞膜包裹巴戟天来源的PELNVs) | 巧妙结合植物囊泡的治疗活性和红细胞膜的免疫逃逸能力,增强疗效 | 工程化纳米囊泡,用于类风湿性关节炎的治疗 |
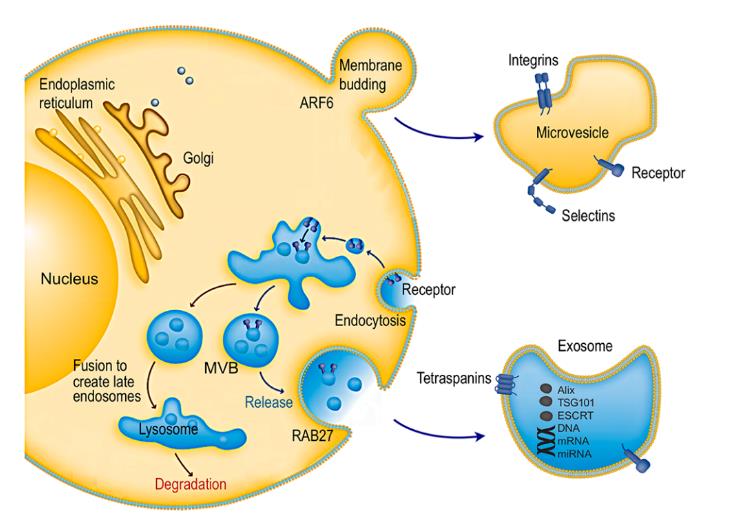
创新工艺的深层逻辑。这些创新并非孤立存在,它们共同指向PELNVs制备的三大趋势:从“粗放提取”到“精细制备”:早期的制备方法可能更注重“得到”囊泡。而现在的创新,如酶解法和优化的超声法,更注重如何在提取或载药过程中保持囊泡的天然结构和功能完整性,减少损伤,为后续应用打下坚实基础。从“通用载体”到“智能导弹”:单纯的PELNVs本身具有一定的被动靶向性。但通过靶向修饰(如Wnt3a蛋白)和仿生膜包裹(如红细胞膜)等技术创新,研究者正试图给这些囊泡装上“导航系统”,使其能精准识别并富集于病变部位,大大提升治疗效果并降低副作用。从“单一活性”到“协同增效”:创新工艺不仅把PELNVs当作“运货卡车”,还充分利用其自身的生物活性。例如,橄榄叶外泌体本身就具有抗炎作用,与它装载的羟基积雪草苷功效协同,实现了“1+1大于2”的效果。这种载体与货物协同治疗的思路,极大拓展了PELNVs的应用潜力。
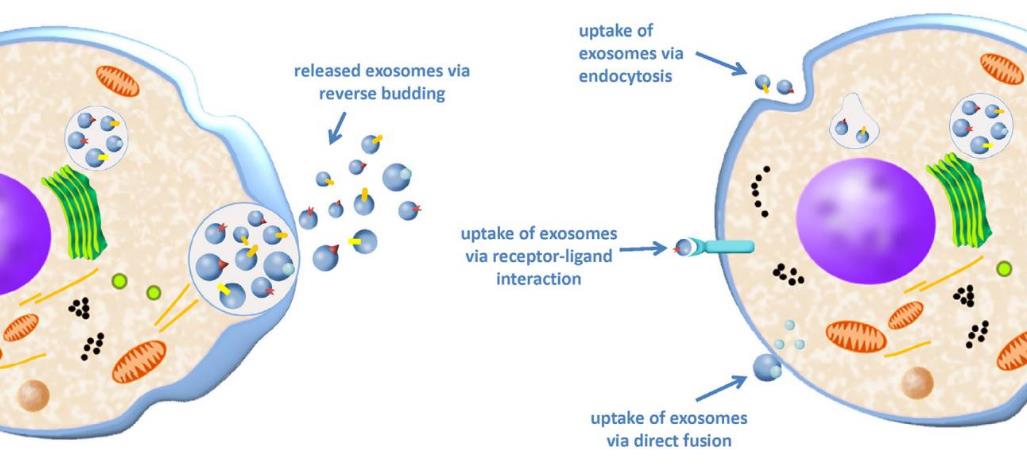
《中草药囊泡研究与应用专家共识(2023年版)》对植物源外泌体样纳米囊泡的分离方法提供了详细的指导。《中草药囊泡研究与应用专家共识》中提到的PELNVs分离方法有几个具体步骤。其核心流程可以概括为以下几个关键阶段,下面图为你清晰展示了从原料到成品的完整路径和主要方法选择。以下是每个环节的具体步骤和关键细节:原料预处理与初级提取。共识特别强调,需根据药材的物理状态(如新鲜/干燥、部位) 选择预处理方式,这是成功分离的第一步。新鲜多汁的原料:如生姜、韭菜的叶类。通常采用榨汁或压榨的方式获取汁液。干燥或汁液不多的原料:如苍术根等根茎类药材。常用煎煮法(如苍术根加水煮沸30分钟)或研磨后提取,以将有效成分充分释放到水相或缓冲液中。
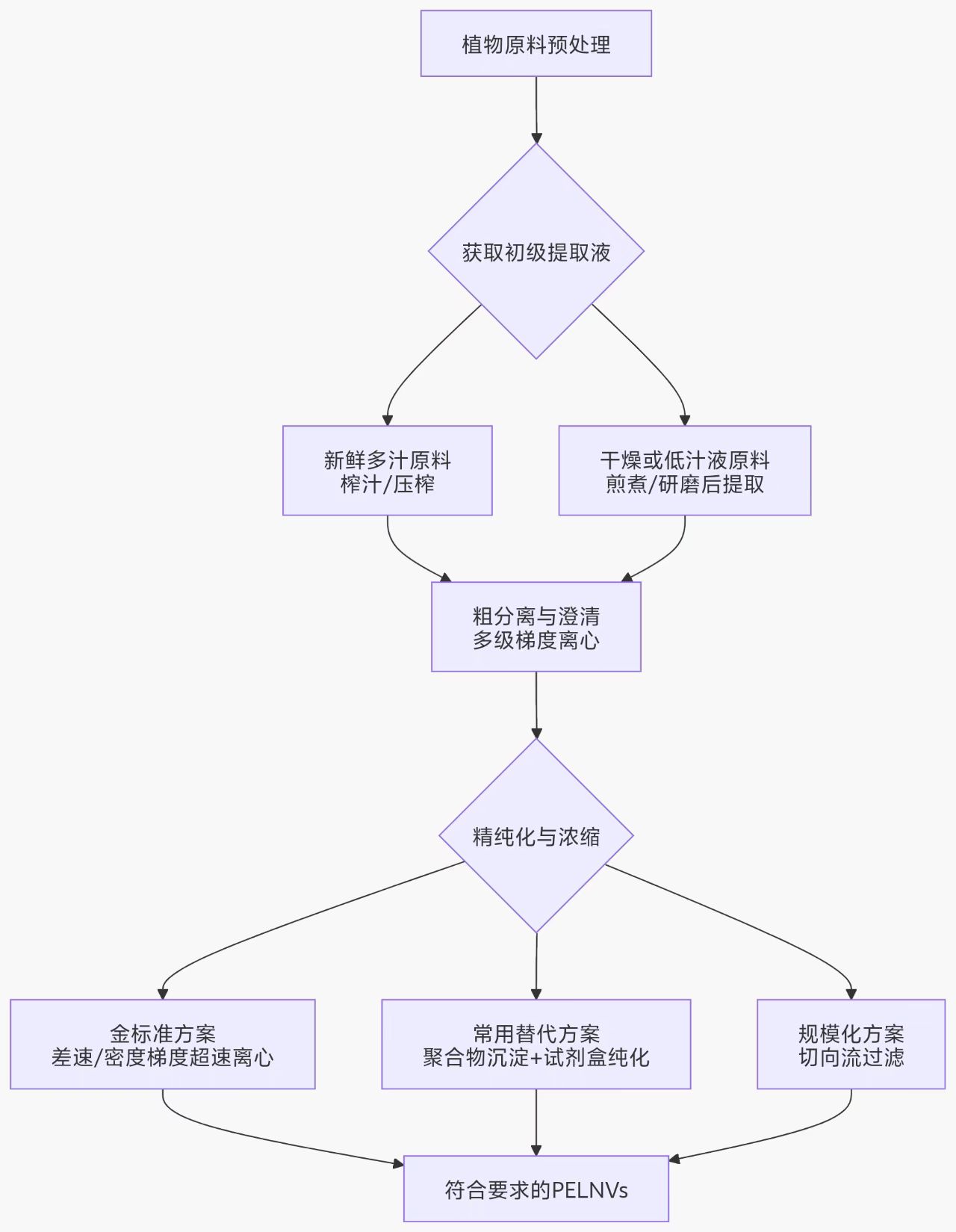
粗分离与澄清。获取初级提取液后,核心目标是去除大的细胞碎片和组织残渣。此步骤通常通过系列梯度离心完成:低速离心:例如在 1,000 - 2,000 × g 下离心10-15分钟,目的是去除较大的植物细胞碎片。中速离心:随后在更高的离心力下,如 4,500 - 15,000 × g,离心20-30分钟,以进一步清除更小的颗粒和杂质。微孔过滤:将上清液通过 0.45 μm 或 0.8 μm 的微孔滤膜进行过滤,获得相对澄清的液体,为后续的高纯度制备做准备。精纯化与浓缩。这是获得高纯度PELNVs制品的核心步骤,共识和最新研究中提到了几种主流方法:差速超速离心与密度梯度离心:这种方法被视为分离的“金标准”。通过高达 100,000 × g 以上的超高速离心,可以将PELNVs沉淀下来。为进一步提高纯度,常结合蔗糖密度梯度离心,使囊泡在特定密度区间(如30%-45%蔗糖浓度)富集,从而与可溶性蛋白等杂质分离。聚合物沉淀与试剂盒纯化:这是一种非常常用的方法,特别适合实验室快速操作。

在澄清液中加入聚乙二醇(PEG,如PEG-6000) 至一定浓度(如8%-15%),在低温(如2-8℃)下静置过夜,使PELNVs发生沉淀。然后通过相对低速度的离心(如8,000 × g)收集沉淀。沉淀可用缓冲液重悬,并可进一步使用商业化的提取试剂盒(如exoEasy Maxi Kit)进行纯化。切向流过滤:这是一种新兴的、适合规模化制备的技术。其原理是利用切向的流体剪切力,使样品平行流过滤膜表面,将PELNVs保留在系统内,而小分子杂质则透过膜被除去,从而实现高效浓缩和缓冲液置换。这种方法处理量大、操作温和,能更好地保持囊泡的完整性,且易于线性放大,符合未来工业化生产的需求。

关键操作要点。在操作过程中,有几个要点对保证PELNVs的质量至关重要:低温环境:除非步骤特殊需要,整个分离过程建议在 4℃ 的低温环境下进行,以防止囊泡降解并抑制微生物生长。质量控制:共识建议,最终制备的PELNVs应通过透射电子显微镜 观察其典型的杯状或球形形态,并使用纳米颗粒跟踪分析 技术测定其粒径分布(通常为30-200 nm)和颗粒浓度。
验证植物源外泌体样纳米囊泡(PELNVs)制备工艺的稳定性和批间一致性,是其从研究走向应用的关键。这需要一套系统的质量控制策略,主要围绕物理属性、生化成分、生物功能及稳定性这几个核心维度展开。需要关注的关键指标和常用的评估方法。
验证维度 | 关键指标 | 评估方法与合格标准 |
物理属性一致性
| 粒径分布与颗粒浓度 | 使用纳米颗粒跟踪分析(NTA)或动态光散射(DLS)检测。批间一致性要求:中位粒径偏差通常应<10%-15%,颗粒浓度应在同一数量级内波动。 |
颗粒形态 | 通过透射电子显微镜(TEM)观察,确保不同批次样品中均可见完整的、呈杯状或球形的囊泡结构,无明显碎片或杂质。 | |
生化成分一致性
| 蛋白质组成
| 通过BCA法等测定总蛋白含量,并计算总蛋白与颗粒数的比值。该比值在不同批次间应保持稳定。通过SDS-PAGE电泳观察蛋白条带图谱,确保主要条带一致。 |
特定标志物
| 利用Western Blot、ELISA或质谱技术检测已知的PELNVs相关蛋白(如HSP70),确保其在各批次中均能稳定检出。 | |
核酸特征
| 提取总RNA,通过微量核酸分析仪测定其浓度和质量。对小RNA进行测序分析,确保不同批次具有相似的RNA谱系特征。 | |
工艺参数稳定性 | 关键步骤参数 | 对分离纯化中的关键参数(如超速离心转速时间、超滤膜截留分子量、色谱柱保留时间等)进行监控和记录,确保其严格控制在标准范围内。 |
中间品控制 | 对关键工艺步骤后的中间品(如澄清后的汁液、浓缩后的样品)进行上述理化指标的快检,实现过程控制。 | |
稳定性与功能验证 | 加速与长期稳定性
| 进行加速稳定性试验(如反复冻融、不同温度储存)和长期留样观察。定期检测颗粒粒径、浓度和蛋白含量等指标,以确定最佳储存条件和有效期。 |
生物活性/功能 | 根据PELNVs的预期用途(如药物递送、抗炎),设计体外或体内生物活性实验。批间一致的产品应表现出可重现的生物效应。 |
如何建立验证体系。要系统地进行验证,建议你遵循以下步骤:建立标准操作规程(SOP):这是所有工作的基础。必须为原料前处理、分离纯化、检测方法等每个环节制定详尽的SOP,确保每次操作都一致。定义参比标准品:选择一批制备工艺成熟、质量指标优异的PELNVs样品作为“参比标准品”(或“黄金批次”),与后续的生产批次进行对比,使评估有基准可循。实施统计过程控制(SPC):在工艺稳定阶段,连续制备多批(例如5-10批)样品,收集关键质量属性(CQA)数据。计算这些数据的平均值和标准偏差,并以此设置合理的控制限(如±2σ或±3σ)。未来生产的批次,其质量指标应落在控制限内。进行稳定性研究:定期从留样批次中取样,检测关键指标的变化,从而科学地确定产品的储存条件和有效期。
核心要点提醒。风险控制:识别工艺中的关键质量属性(CQAs)和关键工艺参数(CPPs),并进行重点监控。持续改进:验证是一个持续的过程。当原料、设备或工艺发生任何重大变更时,都需要重新进行验证。记录完整:详尽、准确的生产和检验记录是进行追溯和根本原因分析的基础。这些信息能帮助系统地构建PELNVs的工艺验证方案。

ISO/TC276(生物技术)委员会为细胞外囊泡的研究提供了重要的框架和指导,其核心在于建立一套通用、可靠且可重复的检测方法体系。虽然其标准主要基于动物和人体细胞外囊泡的研究,但其确立的原则和方法对PELNVs的检测有非常重要的参考价值。表格概括了ISO/TC276标准框架下对EVs(包括PELNVs)检测方法的核心建议。
检测维度 | 核心建议方法 | 主要技术参数与目的 |
颗粒物理表征 | 纳米颗粒跟踪分析 (NTA) | 测量颗粒浓度(颗粒数/mL)和粒径分布。用于确定样本中囊泡的绝对浓度和大小均一性。 |
动态光散射 (DLS)
| 快速测量颗粒的平均流体动力学直径。适用于评估样本的单分散性,但对混合物不敏感。 | |
可调电阻脉冲传感 (TRPS) | 在高分辨率下测量单个颗粒的粒径和浓度,能有效分析异质性样本。 | |
电子显微镜 (EM/TEM) | 直接观察囊泡的形态、结构(如典型的杯状结构)和大小,提供直观证据。 | |
生化成分分析 | 蛋白质印迹法 (Western Blot) | 鉴定特异性或相关性蛋白标志物的存在(如跨膜蛋白CD63、热休克蛋白HSP70等)。 |
流式细胞术 | 对单个囊泡或囊泡群体进行表面标志物的定量和表型分析。 | |
蛋白质组学(如质谱法) | 无偏向性地全面分析囊泡携带的蛋白质组成,有助于发现新的标志物。 | |
纯度与杂质评估 | 总蛋白/总颗粒数比值 | 评估样本的相对纯度,比值过高可能提示存在非囊泡蛋白污染。 |
特定污染物检测
| 检测载脂蛋白(常见于血清样本)、核酸酶等,确保样本不含特定杂质。 |
核心原则与PELNVs的特殊考量。ISO/TC276标准的核心精神是通过多种互补的技术手段(MSEV指南强调至少两种不同原理的方法)来综合鉴定囊泡,避免因单一方法的局限性导致误判。在将这套框架应用于PELNVs时,需要特别注意以下几点:标志物的差异:动物细胞外泌体的经典标志物(如CD9、CD63、CD81)在植物中可能并不存在或表达模式不同。因此,直接套用这些标志物来鉴定PELNVs是不科学的。目前的研究更倾向于寻找植物来源的特有蛋白(如一些质膜ATP酶、特定热休克蛋白等),或依靠物理表征(粒径、形态)和通用生化指标(总脂质、总RNA含量)进行综合鉴定。杂质来源的特殊性:PELNVs制备过程中,除了常见的细胞碎片和游离蛋白污染,还需特别关注植物源性杂质,如叶绿素、色素、植物次生代谢产物(如多酚)等。这些杂质可能干扰后续的检测和分析,需要在质量控制中加以考量。功能性检测的纳入:标准鼓励根据应用目的设计功能性检测。例如,若PELNVs旨在用于药物递送,则应评估其载药量、包封率和靶向细胞摄取效率等。

实施建议与挑战。对于PELNVs的研究者和生产者而言,遵循ISO/TC276的建议意味着:建立内部质量控制程序:在实验室内部,应为每一项关键检测指标(如NTA测浓度、Western Blot检测标志物)建立标准操作程序,并定期使用标准品或参考物质对仪器和方法进行校准和验证,以确保结果的准确性和可比性。应对技术挑战:PELNVs的异质性、提取工艺的差异以及目前缺乏公认的植物源外泌体标准品是当前面临的主要挑战。这使得不同实验室、不同批次产品之间的数据比较变得困难。总而言之,ISO/TC276标准为PELNVs的检测提供了严谨的方法学框架和最佳实践指南。虽然在实际应用中需要根据植物来源的特殊性进行调整(尤其是标志物选择),但其强调的多参数、正交性验证的核心原则,是确保PELNVs研究成果可靠、数据可比、产品质量可控的基石。
制定植物源外泌体样纳米囊泡(PELNVs)标准草案中的性能指标数值范围,是一个需要科学基础、行业共识和实用考量相结合的过程。它旨在确保产品安全、有效、质量可控,同时为行业提供明确的准入门槛和测试依据。确立核心指标与设定思路。下表概括了PELNVs标准草案中应考虑的核心性能指标类别及设定其数值范围的基本思路
指标类别 | 核心指标 | 设定数值范围的主要考量因素与方法
|
物理特性 | 粒径分布
| 基于NTA等技术的测量数据,范围通常设定在30-200 nm。需规定主峰占比(如>80%)和多分散指数(PDI,如<0.3)以确保均一性。 |
颗粒浓度 | 根据制备工艺(如超速离心、切向流过滤)水平,设定每毫升溶液中的颗粒数范围(例如10^8 - 10^12 particles/mL),并为不同应用(科研、化妆品、医药)设定不同等级。 | |
化学组成
| 纯度(颗粒/蛋白比) | 通过BCA法测总蛋白,结合NTA颗粒数,计算比值(如>3×10^10 particles/mg protein),以控制游离蛋白等杂质。
|
特定标志物
| 对于已明确的植物外泌体标志蛋白(如HSP70、PEN1),规定Western Blot检测应为阳性;对植物细胞胞质杂质蛋白(如RuBisCO),规定应为阴性。 | |
生物活性
| 生物活性测定
| 根据PELNVs来源(如生姜抗炎、葡萄柚修复)和预期用途,建立体外细胞模型(如抑制炎症因子IL-6释放≥30%)或生化检测(如DPPH自由基清除率≥70%)的活性标准。 |
安全性 | 无菌检查 &内毒素 | 注射用必须无菌、内毒素极低(如<0.5 EU/mL);口服/化妆品级需符合相应微生物限度标准(如菌落总数<100 CFU/mL)。 |
外源性污染物 | 严格限定重金属(如铅<1 ppm)、农药残留(如总农残<10 ppm)和溶剂残留等,需符合药品/食品/化妆品原料的通用安全标准。 |

制定过程中的关键步骤。确定上述指标和范围不是一蹴而就的,以下几步至关重要:广泛收集数据:这是科学设定的基础。需要大量收集不同实验室、不同制备方法、不同植物来源的PELNVs的检测数据。这些数据可以帮助了解各指标的自然波动范围。参考现有指南与共识:积极采纳《中草药囊泡研究与应用专家共识(2023年版)》和国际细胞外囊泡学会(ISEV)的MISEV指南等已有权威文件中的建议值,能提高标准草案的科学性和国际认可度。进行方法学验证:在确定指标范围前,必须确保所用的检测方法(如NTA、BCA、HPLC)本身是可靠、可重复的。这包括确定方法的精确度、准确度、线性范围等。例如,有研究指出开发新型色谱柱(如EVscore系列)可以更好地定量检测PELNVs中的杂质。 
基于风险和应用分级:不同用途的PELNVs对指标的要求严格程度不同。标准草案可以考虑分级制度。例如,用于科学研究的PELNVs,其纯度要求可以比直接注射入人体的药用级PELNVs更宽松。行业研讨与共识建设:组织由科研机构、生产企业、监管部门和检测单位专家参与的研讨会,对初步设定的数值范围进行充分讨论和修订,最终达成行业共识,这能极大地增强标准的可执行性。在标准草案中的规范表述。在标准草案的文本中,每个性能指标的数值范围都应清晰、无歧义地表述。通常采用以下格式:【指标名称】:应明确测试方法。例如,“粒径分布:采用纳米颗粒跟踪分析(NTA)法测定。中位粒径(D50)应在30-150 nm范围内,且多分散指数(PDI)应不大于0.3。”对于某些暂时无法确定固定数值的指标,可以规定其稳定性要求,例如:“生物活性:各批次产品应保持稳定的生物活性,其效价与参比品比较应在80%-120%范围内。”

验证植物源外泌体样纳米囊泡(PELNVs)检测方法的准确度,是确保其测量结果真实可靠的核心环节。表格汇总了主要的验证维度和常见方法。
验证维度 | 核心目标 | 常用方法与策略 |
准确度 (Accuracy) | 衡量测量平均值与真实值的接近程度 | 回收率实验 (Recovery Test)、方法学比对
|
精密度 (Precision) | 衡量多次独立测量结果之间的一致性 | 重复性 (批内精密度)、再现性 (批间精密度) |
线性与范围
| 确定检测结果与被测物浓度成比例的范围 | 使用高、低浓度样品按比例稀释,制备至少5个不同浓度的样本进行测定 |
特异性 | 评估方法区分PELNVs与干扰物质的能力 | 通过检测可能存在的杂质(如植物色素、多酚等),观察其对检测结果的干扰程度 |
准确度的核心:回收率实验。回收率实验是评估方法准确度最直接的手段,尤其适用于成分复杂的PELNVs样品。其核心思路是在已知本底的样品中加入已知量的待测物,通过测定加入物能否被定量“回收”来判断准确度。回收率包括绝对回收率和相对回收率。绝对回收率:主要考察样品处理过程中的损失。它是将空白基质中加入标准品后经完整样品处理所得的结果,与直接用溶剂配制相同浓度标准品所得结果的比值。此比率反映样品处理(如离心、过滤)造成的目标物损失,一般要求大于50% 。
相对回收率(加样回收率):更侧重于考察方法的准确度。这是在已知浓度的真实PELNVs样品中,加入一定量的PELNVs标准品或已知浓度的另一份PELNVs样品,然后用待验证的方法进行测定。计算实测值与“理论值”(原样品含量与加入量之和)的比值。相对回收率的计算公式为:回收率(%) = (加标试样测定值 - 试样测定值) / 加入量 × 100% 。一个理想的方法,其回收率应接近100%,通常在95%-105% 之间被认为是可接受的。
回收率实验设计要点。样品与加标物选择:基础样品:最好使用特性明确的PELNVs样品或经过充分表征的PELNVs标准品。加标物:理想情况下,应使用与基础样品来源相同、制备方式一致的PELNVs浓缩液作为加标物。如果条件有限,也可使用经过充分验证的PELNVs标准品。浓度水平设计:应至少设计3个不同的添加浓度,建议覆盖样品的预期浓度范围,例如80%, 100%, 120% 的浓度水平,这有助于评估方法在不同浓度下的准确性。操作注意事项:加标体积应尽可能小,通常不超过总体积的10%,以避免过度稀释基础样品。每个浓度水平应进行多次平行测定(通常不少于3次),并计算平均值和相对标准偏差(RSD),以同时考察精密度。

其他关键验证指标。一个可靠的检测方法,除了准确度,还需验证其他几项关键性能指标:精密度:指在规定的测试条件下,同一均匀样品多次取样测量结果之间的一致程度。重复性:在相同条件下(同一操作员、同一设备、短时间)对同一样品进行多次测量的一致性。再现性:在不同条件下(不同实验室、不同操作员、不同设备)对同一样品进行测量的一致性。精密度通常以标准差或相对标准偏差表示。线性范围:指检测方法的检测结果与样品中被测物的浓度成比例关系的范围。应通过实验确定方法的线性范围,并确保待测样品的浓度落在该范围内。特异性:指检测方法能够准确、专一地测量PELNVs的能力,评估是否存在干扰。对于PELNVs,需要特别关注植物次生代谢产物等杂质的干扰 。

总结与实施路径。总的来说,验证PELNVs检测方法的准确度是一个系统工程,回收率实验是评估准确度的核心,但必须与精密度、线性等其他指标协同验证。建议可以按照以下路径开展:明确检测目标:首先确定您需要定量检测PELNVs的哪些属性(如粒径分布、颗粒浓度、特定蛋白含量等)。设计回收率实验:参照上述要点,为您的目标属性设计严谨的加样回收实验。全面验证:按照表格所列的维度,对方法的精密度、线性等指标进行系统验证。参考专家共识:在进行相关研究时,可以参考《中草药囊泡研究与应用专家共识》等文件,以了解领域内的常见做法和建议 。

植物源外泌体样纳米囊泡(PELNVs)的检测技术近年来发展很快,核心进展集中在让检测更精准、更全面、更贴近其生物学功能。
检测维度 | 核心进展 | 关键技术/方法 | 解决的核心问题 |
物理性质表征
| 单颗粒水平的多参数同步分析 | 电阻脉冲传感(RPS)技术,如NanoCoulter仪器
| 在一次检测中同时获取单个颗粒的粒径和Zeta电位,揭示群体的异质性,而不仅仅是平均结果。 |
形态学与成分鉴定 | 高分辨率成像与组分精准定量
| 冷冻透射电镜(Cryo-TEM)、BCA蛋白定量与纳米颗粒跟踪分析(NTA)联用 | 更真实地观察囊泡原始形态,并通过总蛋白与颗粒数的比值等指标客观评估样品纯度,减少主观判断误差。 |
功能活性验证 | 从“有什么”到“能干什么”
| 细胞摄取实验、特定疾病模型(如骨关节炎)下的功能基因表达分析(qPCR)
| 直接验证PELNVs被目标细胞摄取的能力及其后续的抗炎、抗氧化、促进修复等生物效应,链接结构与功能。 |
植物来源特异性检测 | 应对标志物缺乏的挑战
| 跨物种通用表征方案(电镜+NTA+功能验证),避免直接套用动物源标志物 | 在植物源外泌体特异性蛋白标志物不明、商业化抗体稀缺的情况下,建立可靠的质量控制体系。 |

技术进展的深层解读。从“群体平均”到“单颗粒视角”。传统动态光散射等技术提供的是一系列颗粒的平均值。而像NanoCoulter这类基于电阻脉冲传感的技术,能逐个分析颗粒,并生成粒径-电位的二维散点图。这能清晰展示样品中是否存在不同亚群,对于评估制备工艺的稳定性和发现具有特定功能的囊泡亚群至关重要。多技术联用成为“金标准”。单一方法已无法满足严谨的鉴定需求。当前趋势是采用正交互补的策略。例如,一项关于葡萄柚来源囊泡的研究中,研究者系统性地联合使用了NTA、透射电镜、BCA法等方法,并进行了细胞功能实验。这种“组合拳”能相互验证,确保检测结果的可靠性,正成为高质量研究的标配。

功能检测驱动应用转化。最新的研究越来越注重证明PELNVs的生物学效应。例如,通过荧光标记直接观察囊泡被软骨细胞摄取的过程,并通过qPCR检测其处理后炎症、抗氧化、软骨再生相关基因的表达变化。这直接将PELNVs的物理化学特性与其潜在的治疗价值联系起来,为药品、化妆品等应用领域的功效宣称提供了直接证据。特殊挑战与应对。植物源外泌体有一个显著特点:缺乏像动物源外泌体CD63、CD81那样公认的特异性蛋白标志物。因此,Western Blot在此领域应用受限。目前的共识是,不强行套用动物标志物,而是依靠电镜形态观察、NTA粒径分析、功能蛋白活性检测等通用表征手段,结合细胞功能实验进行综合鉴定。

总结与展望。总的来说,PELNVs检测的最新进展体现在:检测精度:从群体测量进入单颗粒分析时代。检测策略:从单一方法转向多技术正交验证。检测目的:从单纯的物理表征深入到生物功能验证。未来,随着对植物源外泌体特有标志物的不断发现,以及微流控等自动化高通量技术的应用,PELNVs的检测将朝着更标准化、精细化的方向发展。



