

撰写一份专业的PELNVs制备工艺验证报告,是证明您的工艺稳定、可靠且符合规范的关键一步。下面将结合报告的核心结构和PELNVs的特性,提供一个清晰的撰写指南。报告的核心结构。一份完整的工艺验证报告通常包括以下部分
报告章节 | 核心内容与PELNVs特别关注点 |
1.报告摘要
| 简要说明验证目的、批次、关键结论(如工艺是否稳定、批间一致性是否达标)。 |
2.验证背景与目的 | 阐述验证的必要性,明确验证要证明的具体目标(例如:“确认XX制备工艺能连续三批生产出符合预设质量的PELNVs”)。 |
3.验证范围 | 明确界定验证覆盖的工艺环节(如从植物材料前处理到超速离心纯化的全过程)。 |
4.验证依据 | 列出所遵循的法规、指南、内部质量标准或参考文献。 |
5.验证小组及职责 | 明确参与验证的各职能部门(如研发、生产、QA、QC)及个人职责。 |
6.材料与方法
| • 制备工艺简述:描述完整的工艺流程,最好附上流程图。• 主要设备与试剂:列出关键设备(如超速离心机、NTA仪器等)及其校准状态。• 验证批次信息:明确验证批次的批号、生产日期、规模等。 |
7.验证结果与分析(核心章节) | 这是报告的灵魂,需要分模块呈现数据并与预设的可接受标准进行对比。 |

下表详细说明了第7章中应包含的典型验证内容及PELNVs的关键指标:
验证维度 | 验证内容 | PELNVs关键指标与可接受标准示例 |
物理属性
| 粒径分布、颗粒浓度、Zeta电位、形态
| • 粒径:三批产品的平均粒径应在预设范围(如100±20 nm)内,多分散指数(PDI)小于0.3。• 颗粒浓度:批间差异应小于15%。• 形态:TEM图像显示典型的杯状形态,结构完整。 |
生化成分 | 蛋白质含量、特定标志物、核酸特征
| • 蛋白/颗粒比值:批间RSD应小于20%。• 标志蛋白:Western Blot检测到TSG101等特异性标志物。• RNA谱:电泳显示典型的小RNA条带。 |
工艺过程 | 关键工艺参数(CPP)监控、中间品控制 | 记录并确认各批次的关键步骤(如离心力、过滤条件)参数均在控制范围内。 |
无菌及内毒素 | 无菌检查、内毒素含量 | 符合注射级或研究级标准(如内毒素小于0.25 EU/mL)。 |

报告后续章节 | 核心内容 |
8.偏差与变更分析
| 如实记录验证过程中出现的任何偏差,并进行根本原因分析,评估其对产品质量的影响。 |
9.验证结论 | 基于所有数据,明确给出工艺是否验证成功的最终结论。 |
10.再验证建议
| 明确在何种情况下需要启动再验证(如主要原料变更、关键设备更替等)。 |
11.附件
| 附上原始数据记录、代表性图谱(如NTA粒径分布图、TEM照片)、仪器校准证书等。 |

让报告更专业的实用建议。数据呈现要直观:多使用表格和图表(如折线图展示三批粒径趋势,柱状图对比收率),让数据对比一目了然。结论要基于数据:避免使用“可能”“大概”等模糊词汇。结论应直接源于数据与预设标准的客观比较。团队评审确保严谨:报告在最终批准前,应经过验证小组所有关键成员(如生产负责人、质量负责人)的评审和会签,确保其准确性和公正性。PELNVs的特殊考量:鉴于PELNVs的来源多样且研究仍在深入,报告中应特别说明其植物来源、为减少宿主植物成分残留所采取的控制措施,以及相关的生物安全性数据(如果适用)。持续工艺验证。工艺验证并非一劳永逸。在商业化生产阶段,应建立持续工艺确证体系,通过持续监控关键工艺参数和关键质量属性,确保工艺始终处于受控状态。

在制定PELNVs(植物源外泌体样纳米囊泡)标准草案时,为检测报告建立一个统一、严谨且信息完备的格式至关重要。这不仅是质量控制的最终体现,也是确保数据可追溯、可比较的关键。一份规范的PELNVs检测报告,其核心框架和应包含的信息点可以用下面的图表来清晰展示:形成一份具有法律效力和科学价值的完整检测报告。
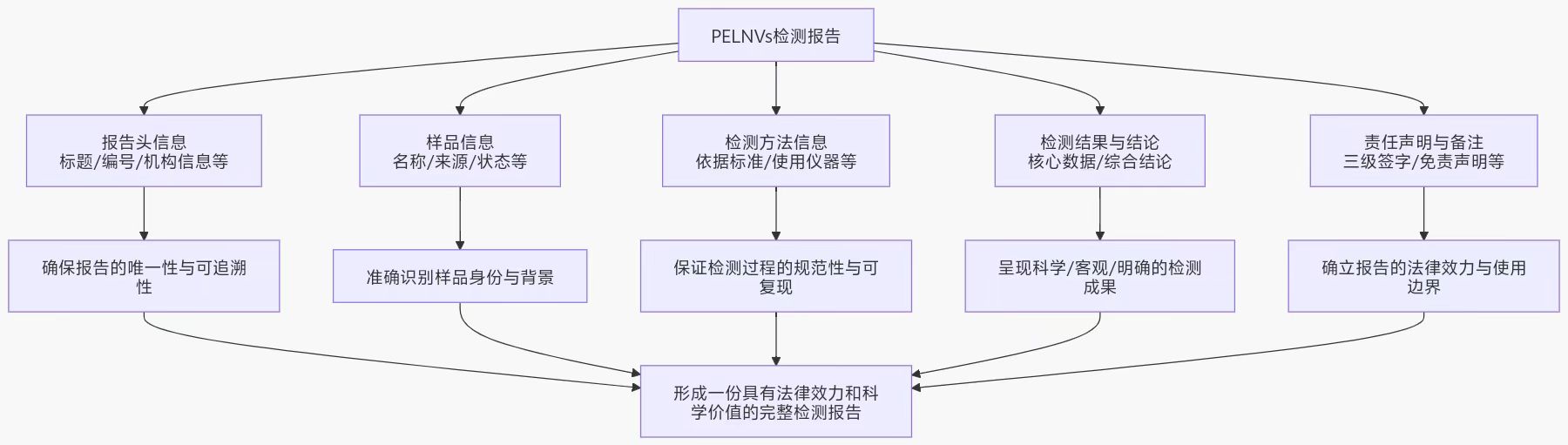
报告核心内容详解。图展示了报告的骨架,而填充这些部分的具体要求如下:1.报告头信息。这是报告的“身份证”,用于唯一识别和追溯。应包括:报告标题:明确为“植物源外泌体样纳米囊泡(PELNVs)检测报告”。唯一性编号:便于档案管理和查询。检测机构信息:机构全称、地址、联系电话等。报告日期与页码:注明报告签发日期和总页数-第X页。2.样品信息。详尽的样品信息是结果准确的前提。应涵盖:样品背景:名称、植物来源、提供单位、生产/批次号。样品状态:接收时样品的物理状态、包装、数量等信息。关键日期:样品接收日期和检测日期。

3.检测方法与条件。此部分证明检测过程的科学性。需明确:检测依据:写明遵循的标准方法(如本标准草案编号)、参考文献或经过验证的非标方法。主要设备与环境:列出所用关键仪器(如NTA仪、TEM型号)及其校准状态,以及重要的环境条件(如温度、湿度)。4.检测结果与结论。这是报告的核心,必须清晰、客观、准确。结果呈现:建议多采用表格形式,列明检测项目、标准要求、检测结果和单项结论。对于PELNVs,关键指标通常包括:形态学:提供TEM图像,描述囊泡形态(如杯状)。粒径与浓度:通过NTA检测,报告平均粒径、粒径分布(如D50、D90)和颗粒浓度。标志物特征:如通过蛋白质印迹法(Western Blot)检测特定蛋白的表达情况。纯度评估:例如,计算颗粒数-总蛋白比值等。检测结论:结论应基于数据,明确说明样品是否符合既定标准或合同要求,避免模棱两可的表述。

5.责任声明、备注与签署。这部分规定了报告的法律效力和使用边界。重要声明:通常包括“报告无专用章或公章无效”、“报告涂改无效”、“异议申诉期限”(如收到报告15日内提出)等。若为委托检验,需声明“仅对来样负责”。备注项:用于说明对标准方法的偏离、分包情况、测量不确定度等需要特别说明的事项。审批签署:报告需经过制表、审核、批准三级签字或等效标识,批准人应为授权签字人。同时应加盖 “检验报告专用章”。总结为PELNVs制定标准化的检测报告格式,其最终目的是构建一套可靠的质量沟通语言。通过统一格式,可以确保不同批次、不同实验室产生的数据具有可比性和可靠性,为PELNVs的研究、开发、生产与应用打下坚实的基础。

在PELNVs的标准草案中,确保数据的可追溯性是其科学性和实用性的基石,核心在于对数据全生命周期进行系统化管理,确保每一步操作都有据可查。数据可追溯性的核心框架。PELNVs标准草案为确保数据可追溯性,通常会构建一个覆盖数据全生命周期的框架,其核心环节与要求可概括为下表:
生命周期阶段 | 可追溯性核心要求 | 具体实施示例 |
原材料溯源 | 明确记录植物来源、部位、产地、种植加工条件等。 | 记录中药材的基原(如苍术根)、采摘时间地点、干燥或预处理方法。 |
实验操作记录
| 详细记录样品处理、仪器参数、试剂批号、操作人员等。 | 记录离心力(如15000 × g)、离心时间、过滤孔径(如0.8 μm)、提取试剂盒批号。 |
数据采集与关联 | 自动或手动记录原始数据,并将其与样本、流程唯一关联。 | 通过LIMS(实验室信息管理系统)或ELN(电子实验记录本)系统记录并关联数据。 |
变更的审计追踪 | 系统自动记录任何数据的创建、修改、删除操作。 | 记录数据修改的日期、内容、人员,并保存修改前后版本。 |
存储与安全管理 | 安全存储原始数据、过程数据和元数据,并定期备份。 | 规定关键数据(如NTA原始数据、电镜图像)的保留期限,并实施访问权限控制。 |

实现可追溯性的关键支持。上述框架的有效运行,离不开以下技术和体系的支持:信息化系统与审计追踪:采用符合相关规范的信息化系统(如LIMS、ELN)至关重要。这些系统应具备审计追踪功能,能自动、不可篡改地记录下谁、在什么时候、对数据做了什么修改,并保存修改前后的值,以满足实验室质量管理的要求。元数据管理与知识图谱:通过详细定义和记录元数据(例如数据唯一标识符、来源、类型、采集时间),可以为每个数据点提供完整的背景信息。更进一步,可以利用知识图谱技术构建数据资产之间的关联关系图谱,使数据质量问题的来源更加清晰,实现智能化的数据流动监控。

标准化的操作程序:在实验环节,建立并遵循标准化的操作程序是保证数据一致性和可比较性的前提。例如,《中草药囊泡研究与应用专家共识》已为不同类别植物样本的预处理提供了指导性意见,这为建立统一的原材料处理标准奠定了基础。落地实施建议。在标准草案的落地过程中,可以关注以下几点以确保可追溯性要求切实可行:采用“核心-分级”要求:明确哪些是必须满足的核心可追溯性要求(如关键工艺参数记录、审计追踪),哪些可根据产品研发阶段或应用场景(如科研、化妆品、药品)实行分级管理。明确技术实现路径:标准可推荐或规定实现可追溯性的技术方法,例如使用具备审计追踪功能的电子记录系统取代纸质记录,以确保记录的完整与真实。强调数据生命周期管理:将可追溯性融入数据的整个生命周期,从生成、处理、分析到归档乃至销毁,都应有明确的规范,确保数据在任一环节的状态都可查。

最后提供一份结合了行业共识与前沿研究的PELNVs检测报告模板,它综合了通用要素和PELNVs的特殊要求,可以根据具体情况进行调整和使用。
植物源外泌体样纳米囊泡(PELNVs)检测报告
报告编号: PELNVs-2023-001
检测类别: 委托检测/型式检验/科研鉴定
1. 报告概述
项目 | 内容 |
检测机构名称 | [填写检测单位全称] |
检测机构地址/联系方式 | [填写详细地址、电话、邮箱]
|
样品名称 | [例如:生姜源外泌体样纳米囊泡冻干粉] |
规格型号/批号 | [例如:1mL/支;批次:20231108] |
生产日期/有效期 | [具体日期] |
送检单位 | [填写送检单位全称] |
送检日期 | 年 月 日 |
检测日期 | 年 月 日 |
检测依据 | 1.本标准草案(或参考《中草药囊泡研究与应用专家共识(2023年版)》);2. 相关ISO标准(如ISO 22412:2017动态光散射法、ISO 19430:2024 NTA法);3. 内部经过验证的标准操作规程(SOP)。 |
2.检测目的
为确保本品在[药品/保健食品/化妆品]研发与生产中的质量可控性,本次检测旨在对[样品名称]的物理属性、生化成分、纯度及安全性等关键质量指标进行综合表征与评价。
3.样品信息与处理方法
植物来源: [明确到植物的拉丁学名及使用部位,例如:Zingiber officinale (生姜) 根茎]。
制备工艺简述: [简述关键步骤,例如:采用差速离心结合蔗糖密度梯度离心法,或某商业化提取试剂盒(如exoEasy Maxi Kit)进行分离纯化]。
样品状态描述: [例如:液态制剂,呈淡黄色透明液体,无肉眼可见沉淀物]。
4.检测方法与结果
以下是最关键的检测项目、方法及结果部分,建议以表格形式清晰展示。
检测类别 | 检测项目 | 检测方法
| 标准要求/可接受标准 | 检测结果
| 单项结论 |
物理表征 | 形态观察 | 透射电子显微镜(TEM) | 呈现典型的杯状或茶托状双分子层膜结构 | 提供代表性电镜照片,描述形态 | 合格 |
粒径分布
| 纳米颗粒跟踪分析(NTA)
| D50粒径范围:30-150 nm;多分散指数(PDI)小于0.3 | 例如:中位粒径(D50):105 nm;PDI:0.18 | 合格 | |
颗粒浓度 | 纳米颗粒跟踪分析(NTA) | 报告具体浓度(颗粒数/mL) | 例如:3.5 × 10^10 particles/mL | 合格
| |
生化成分与纯度 | 总蛋白含量
| BCA法
| 报告具体数值,并计算蛋白/颗粒比作为纯度参考
| 例如:总蛋白:85 μg/mL;蛋白/颗粒比:~2.4 × 10^3 | 合格 |
特异性标志物 | 蛋白质免疫印(Western Blot) | 检测植物EVs常见蛋白(如HSP70)应为阳性 | 例如:HSP70检测为阳性
| 合格
| |
核酸特性 | 微量核酸分析仪/小RNA测序 | 报告总RNA含量,或小RNA分布特征 | 例如:总RNA浓度:15 ng/μL
| 合格 | |
安全性指标
| 内毒素
| 鲎试剂法
| 根据应用途径设定,如小于0.5 EU/mL(注射用) | 例如:小于0.25 EU/mL
| 合格
|
微生物限度 | 按《中国药典》通则 | 符合规定
| 符合规定 | 合格
| |
无菌检查(如适用) | 按《中国药典》通则 | 无菌生长
| 无菌生长
| 合格
|

备注:检测结果中“/”表示“不适用”,“-”表示“未检测”。附页包含代表性TEM图像、NTA粒径分布图、Western Blot原始图等。
5.结论。综合上述检测结果:本品粒径分布、形态结构符合PELNVs的典型特征。生化成分与纯度指标符合预定标准。安全性指标符合[药品/化妆品/食品]原料相关要求。综上,该批次植物源外泌体样纳米囊泡(PELNVs)样品的检测结果符合本标准/协议要求。
6.签发信息
检测人: ___________ (签名)
审核人: ___________ (签名)
批准人: ___________ (签名)
签发日期: 年 月 日
(检测报告专用章)
重要声明
本报告无“检测专用章”、无审核/批准人签字无效。
本报告部分复制无效。涂改、缺页无效。
委托检测结果仅对所检测样品负责。
如对检测结果有异议,请于收到报告之日起十个工作日内向本机构提出。



