

全国中草药囊泡研究与应用专家委员会这是一个至关重要的机构。该委员会在2023年牵头发布了 《中草药囊泡研究与应用专家共识(2023年版)》 。这份共识文件针对植物样本的特殊性(如根、茎、叶等不同部位的预处理),为PELNVs的分离和鉴定提供了初步的规范性指导,迈出了标准化的关键第一步。确实是中草药囊泡研究领域一个关键的里程碑。它之所以重要,是因为它首次尝试为这个充满潜力但尚显年轻和混乱的领域,建立起一套统一的“语言系统”和基本规范。
共识的里程碑意义。这份共识的重要性主要体现在三个方面:1.首次统一“游戏规则”:在共识发布之前,这个领域就像是一片充满机遇但缺乏规则的新大陆。不同研究团队对同一种植物来源的纳米囊泡可能有不同的命名,采用的提取、纯化和鉴定方法也五花八门。这使得不同研究团队的数据难以直接比较和验证,严重阻碍了知识的积累和技术的可重复性。这份共识如同第一版“宪法”,为领域建立了基本的对话基础。
2.推动中医药现代化:共识巧妙地将传统中草药“简便验廉”的优势与现代纳米技术、精准医学的理念相结合。它指出中草药囊泡可能是阐明中药传统功效现代科学内涵的关键物质之一,为用现代科学语言阐释中医药原理、推动中医药走向世界架设了桥梁。3.凝聚顶尖智慧,指明方向:共识的制定并非易事,它是由全国中草药囊泡研究与应用专家委员会牵头,汇集了国内该领域近三十位顶尖专家的智慧,通过德尔菲法、共识会议等多种科学方法,经过多轮磋商才最终达成。这本身就是一次大规模的合作动员,不仅解决了当下的问题,更吸引了更多研究者进入这一领域,为未来的持续发展注入了活力。
共识的核心内容与努力。为了建立上述的“游戏规则”,共识在文本上做出了几项关键性的努力,主要集中在标准化和规范化上。下表清晰地展示了共识在几个核心维度上达成的关键统一意见。
规范维度 | 共识达成的关键努力 | 解决的核心问题 |
命名标准化
| 建议统称为“中草药来源EVs样颗粒”,具体植物采用《中国药典》拉丁名加“-EVLP”后缀。 | 解决了以往命名杂乱无章、无法有效交流的困境。
|
方法学梳理 | 系统梳理了差速离心、超滤、尺寸排阻色谱等多种方法,并分析了其优缺点。 | 为研究者选择合适方法提供了清晰指南,促进方法学的规范化。 |
质量控框架 | 建立了涵盖形态、粒径、浓度、纯度(如蛋白颗粒比)等多维度的质量控制指标体系。 | 为评估制备产物的一致性、纯度和质量提供了基本依据。
|
安全性前置
| 明确强调安全性评估是临床应用前的首要考虑。 | 将生物安全性这一关键问题提升到核心位置,引导行业健康发展。 |
除了上表中的要点,共识还做了一项重要的“幕后努力”,即诚实地揭示了领域内存在的挑战和未知。它没有回避问题,而是明确指出了当前存在的瓶颈,例如植物囊泡的生物发生机制尚不明确,以及缺乏公认的特异性蛋白标志物等。这种坦诚的态度为未来的研究指明了需要攻坚克难的方向。总而言之,2023版的《中草药囊泡研究与应用专家共识》更像是一位“奠基者”和“引路人”。它通过建立标准、凝聚共识、指明方向,将一个原本有些“散乱”的前沿领域,引导到了规范化、标准化发展的快车道。虽然前路依然有大量科学和技术问题需要解决,但这份共识无疑为整个领域点亮了一座灯塔,使其后续发展有了可共同遵循的基石。
《中草药囊泡研究与应用专家共识(2023年版)》 确实明确涉及并重点关注了植物源外泌体样纳米囊泡。这份共识将其视为中草药现代化研究的核心对象之一,并为此领域的规范化发展奠定了重要基础。与PELNVs直接相关的核心内容梳理:统一定义与范畴。共识采用了“中草药囊泡” 作为核心术语,其定义明确涵盖了PELNVs。核心范畴:共识明确指出,中草药囊泡包括两大类:严格来源于中草药细胞外液的细胞外囊泡。来源于中草药汁液的外泌体样纳米颗粒。后者即广泛研究的PELNVs,共识承认其制备过程中可能因物理破碎而包含细胞内膜结构衍生的囊泡,这与动物细胞自然分泌的囊泡在来源上有所区别。命名建议:为推进标准化,共识建议对具体的中草药,采用《中国药典》中的标准拉丁名,后缀加“-EVLP”。例如,黄芪来源的便称为 Astragali Radix-derived EV-like particles (AR-EVLP)。
研究方法与质量控制框架。共识着重探讨了PELNVs研究中的关键环节,旨在提升结果的可比性与可靠性。分离方法:针对植物样本的多样性(根、茎、叶、果实等),共识总结了不同的预处理和初级提取方法,并分析了差速离心、超滤等方法的优缺点,为选择适合不同原料的标准化分离流程提供了指导。质量控制:共识强调需要建立多维度的质量控制指标体系,这包括:物理表征:如通过透射电镜观察形态,通过纳米颗粒跟踪分析技术测定粒径分布和浓度。成分分析:如蛋白质组学分析等。纯度要求:例如通过计算总蛋白与颗粒数的比值等指标评估样品纯度。

突出安全性评估。共识将安全性评估置于非常重要的位置,明确指出这是PELNVs走向临床应用前必要且首要的考量。共识指出,对于有长期安全口服历史的中草药,其来源的囊泡口服给药被认为是相对安全的途径。但对于非口服给药途径(如注射),则必须通过严谨的研究来验证其安全性。共识的价值。总而言之,这份共识首次为PELNVs研究领域提供了较为系统的框架,涵盖了从命名、制备到质量控制的核心环节,特别强调了基于中药特色的研究路径和安全性的首要地位,为该领域的规范化和可持续发展奠定了重要基础。

目前国内尚未出台专门针对植物外泌体样纳米囊泡(PELNVs)的强制性或推荐性国家标准。当前的相关实践主要参考《中草药囊泡研究与应用专家共识(2023年版)》 。因此,以下分析将该某标准草案与这份代表当前国内主流技术共识的文件进行比较,主要差异体现在以下几个方面:
比较维度
| 当前国内主流共识/实践 (以《中草药囊泡研究与应用专家共识(2023年版)》为代表) | 某标准草案的主要差异与特点
|
标准化路径
| 专家共识:属于指导性文件,侧重于为科研探索提供框架性建议,强调方法的多样性和灵活性。 | 技术标准:旨在建立统一、规范的技术要求,更侧重于产业的可重复性、可衡量性和质量可控性,为未来产品化、市场化奠定基础。 |
原料处理 | 分类指导:针对不同植物部位(如根、茎、叶)提供了差异化的预处理建议,但未强调建立统一的原料质量规范。 | 源头控制:可能更加强调对植物原料的源头质量控制,例如对原料的产地、种植环境、采收期、农残/重金属限量等提出明确要求。
|
分离纯化 | 方法多样:认可并列举了多种分离方法(如差速离心、试剂盒法等),允许根据研究目的和材料特性进行选择,流程相对灵活。 | 工艺统一:可能倾向于推荐或规定一种或几种标准化、可放大的核心纯化工艺(如特定参数下的差速离心结合尺寸排阻色谱),以减少批次差异。 |
特性表征 | 基础表征:主要依赖透射电镜观察形态和纳米颗粒追踪分析测定粒径与浓度。 | 全面质控:在基础表征之上,很可能增加对囊泡纯度、稳定性、标志性活性成分含量等更具产业应用价值的质控指标。 |
质量控制 | 科研导向:质控重点在于证明提取物为“囊泡”,对批次一致性、杂质限量、活性指标等产业关键要素涉及不深。 | 应用导向:建立更严格的质量标准,可能包括微生物限度、内毒素含量、植物次生代谢产物等杂质控制,并对标志性活性成分(如羟基酪醇)设定含量标准。 |
应用导向 | 机制探索:主要服务于科学研究,旨在验证PELNVs的生物活性、作用机制和作为药物递送载体的潜力。 | 产业落地:标准内容直接指向药品、保健食品、化妆品等具体行业的法规要求,为产品注册、生产许可和市场监管提供技术依据。 |
核心差异总结。简单来说,当前国内的专家共识更像是一张为科研工作者绘制的“探索地图”,鼓励多种路径的创新发现;而该某标准,则旨在为产业界打造一本清晰的“生产与质检操作手册”,其核心差异体现在从“探索可能性”向“确保一致性、安全性与有效性”的转变。对该标准草案的建议。基于以上分析,为了使该标准更具前瞻性和实用性,可以考虑:关注国内进展:在标准编制中,可适当关注并引用国内最新的相关团体标准或技术规范,体现与国内实践的协同。预留发展空间:PELNVs研究发展迅速,标准在保证核心指标明确的同时,可在检测方法、工艺细节等方面保留一定的灵活性,或为未来纳入新指标(如生物活性功能评价方法)预留修订接口。
在制定植物源外泌体样纳米囊泡(PELNVs)的国内标准草案过程中,确实面临不少挑战,这主要是因为它是一个前沿且跨学科的领域。
挑战类别 | 具体挑战点 | 关键难点简述 |
技术与方法 | 原料与工艺的多样性
| 植物种类、部位、生长条件差异大,提取方法(如差速离心、超滤、聚合物沉淀)不统一,难以用单一标准覆盖。 |
鉴定与质量控制的标准化 | 植物外泌体缺乏公认的特异性蛋白标志物,纯度评估(如杂质界定)、活性定量方法未统一。 | |
安全与监管 | 安全性评价体系空白 | 需建立全新的评价框架,评估其生物分布、代谢途径和潜在免疫原性等,传统化学药物评价体系不适用。 |
监管分类与政策缺失 | PELNVs属于全新物质类别,需监管部门明确其属于药品、保健食品还是化妆品,并建立相应审评路径。 | |
产业与转化 | 规模化生产的挑战
| 从实验室级别放大到产业化规模时,如何保持囊泡的完整性、纯度与活性是一大难题,成本控制也是挑战。 |
术语与共识待统一
| 领域内对“植物外泌体”等核心术语的定义尚未完全统一,需先形成行业共识。 |
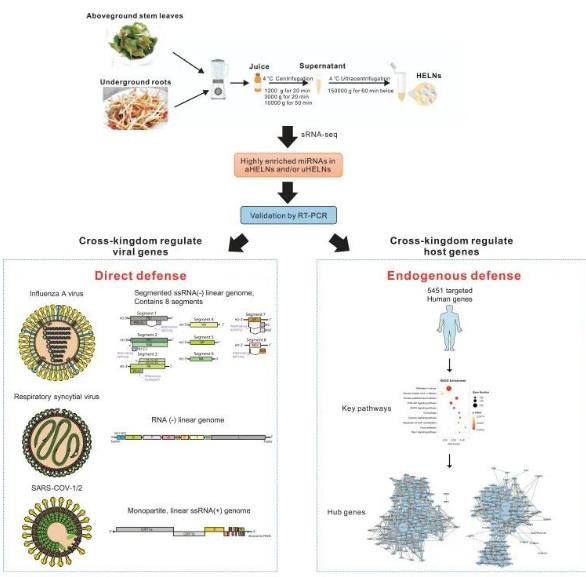
应对挑战的当前努力。面对这些挑战,国内的专家和机构正在积极推动解决。2023年发布的 《中草药囊泡研究与应用专家共识(2023年版)》 是一个重要的里程碑,它针对不同植物原料的预处理方法提供了初步的规范性建议,为标准制定奠定了基础。同时,行业也在积极推动标准化工作,例如中国国际经济技术合作促进会标准化工作委员会已组织召开了《植物外泌体分离纯化工艺技术规范》团体标准的启动会,旨在汇集产学研各方力量,共同攻克关键技术环节的标准化难题。总的来说,PELNVs国内标准草案的制定是一个需要产学研用紧密结合、逐步推进的系统工程。虽然挑战重重,但每解决一个难题,都将为这个新兴领域的规范化和产业化发展扫清一个重要障碍。
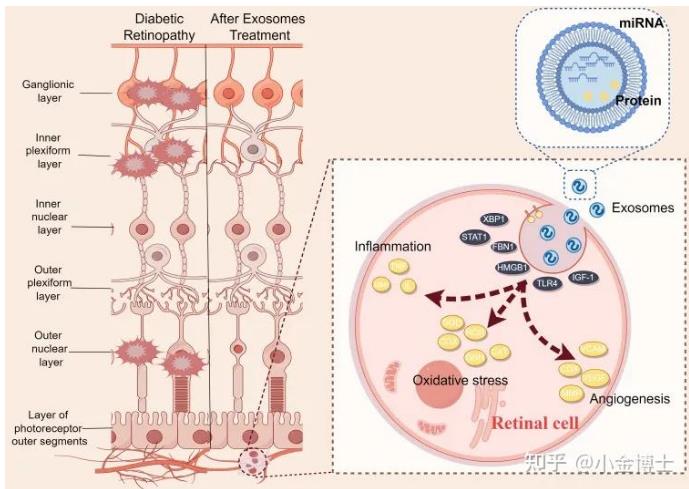
在制定植物源外泌体样纳米囊泡(PELNVs)的某标准草案时,在科学上的严谨与实践中的好用之间找到平衡,确实是核心挑战。一份好的标准,既要能引领技术方向,又要能落地解决实际问题。
平衡维度
| 科学性追求 (确保可靠与先进) | 实用性考量 (确保可行与可用) | 平衡策略建议
|
术语与定义
| 需精确反映PELNVs的生物学本质,与国际术语(如ISEV的MISEV指南)接轨,并明确其与动物源外泌体的异同。 | 术语应简洁明了,便于监管、生产、质检等不同背景的专业人员理解和使用,避免歧义。 | 采纳“植物源外泌体样纳米囊泡(PELNVs)”等已形成共识的术语,并在附录中详细解释其科学内涵和边界。 |
检测方法与指标
| 要求采用多种正交的、可互证的技术(如NTA、TEM、WB等)进行全面表征,指标应能真实反映PELNVs的关键质量属性(CQAs)。
| 方法应考虑到国内多数单位的设备条件,避免将“高精尖”作为唯一标准;同时明确不同用途(如科研、化妆品、医药)可分级采用不同检测套餐。 | 确立“基础指标+特定应用附加指标”的框架。例如,所有PELNVs产品必须检测粒径分布和颗粒浓度,而药用级则需增加无菌、内毒素等严格项目。 |
工艺与质量控制
| 需基于对工艺理解,识别关键工艺参数(CPPs)并建立其与关键质量属性(CQAs)的关联,鼓励采用先进、高效的纯化技术(如TFF)。 | 承认并规范多种制备工艺(如差速离心、聚合物沉淀、超滤等)的适用场景,不“一刀切”地追求单一最优技术,为不同规模的企业提供可行路径。 | 重点规定产物的质量阈值,而非过度限制工艺路径。同时,鼓励并规范替代方法的验证,只要其能达到规定的质量要求。
|
安全性与有效性
| 安全性评价应遵循科学原则,根据给药途径(口服、外用、注射)设定相应的毒理学、免疫原性等研究要求。
| 有效性(活性)评价可引入与预期用途相关的、经过验证的体外生物活性检测方法(如抗炎、抗氧化细胞模型),作为临床前研究的重要补充,使其更易于在研发早期应用。 | 建立基于风险的分类管理原则。对已有长期安全食用历史的植物来源的口服PELNVs,可适当简化部分安全性研究;而对新来源或注射用产品,则需执行最严格的标准。 |
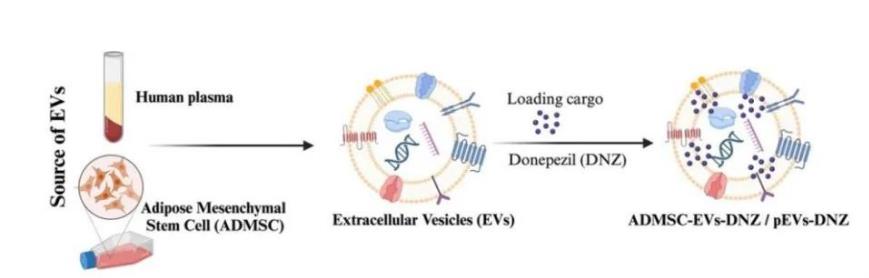
实现平衡的可行路径。要让标准既科学又实用,可以在制定过程中采取以下具体策略:采用“核心规范 + 指导性附录”的弹性结构。将最核心、必须遵守的质量要求作为标准的强制性条款,确保基本的安全性和有效性。同时,将不同制备方法的比较、先进检测技术的原理详解、特定生物活性检测的操作指南等内容,以资料性附录的形式呈现。这既保证了核心标准的简洁和强制力,又为使用者提供了深入理解和工艺优化的丰富参考。建立多方参与的动态修订机制。PELNVs领域发展迅速,标准不应是“一成不变的”。应建立由学术界、产业界、监管机构专家共同组成的标准维护工作组,定期收集实施中的反馈,并关注国际最新科技进展。允许在获得充分证据后,通过标准修改单或新版标准的形式,纳入经实践验证可靠的新技术、新方法,使标准能够持续进化。

强化“性能标准”理念。过于强调“设计标准”(即规定必须使用某种特定设备或工艺)可能会限制创新。应更侧重于“性能标准”(即明确最终产品必须达到的关键质量指标,如纯度、杂质限度、活性强度等)。这样,企业可以选择最适合自身条件的工艺来达标,既鼓励了技术创新,也保证了最终产品的质量。总而言之平衡科学性与实用性的精髓在于 “坚守质量的底线,开放技术的路径” 。一份成功的PELNVs标准草案,应当如同一座坚固的桥梁,其桥墩是科学共识与质量底线,不可动摇;而桥面则足够宽阔和灵活,允许不同用途、不同技术路线的车辆安全高效地通过,最终推动整个行业健康有序地发展。
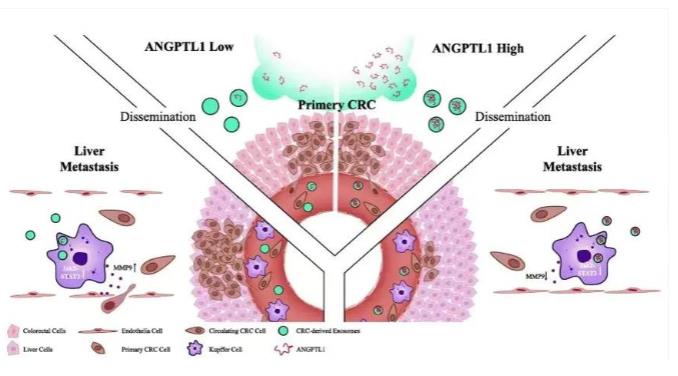
国际细胞外囊泡协会(ISEV)是这一领域的核心推动者。它发布的《细胞外囊泡研究的最低信息要求》(MISEV)指南,虽然主要针对动物源外泌体,但其强调的多技术平台正交验证原则(例如,必须结合形态学、粒径、蛋白标志物等多种方法进行鉴定)为PELNVs的检测提供了重要的基础框架。与国际上较为成熟的动物源细胞外囊泡标准相比,植物源外泌体样纳米囊泡标准在多个方面存在显著的技术考量差异。下表清晰地展示了这些核心差异点。
比较维度 | 国际现有细胞外囊泡标准(以动物源为主) | 该某标准(植物源外泌体样纳米囊泡)的主要差异 |
术语与定义 | 通常明确区分外泌体、微囊泡等亚型,并有相对清晰的生物发生路径。 | 鉴于植物EV亚型和生物发生途径尚不完全明确,建议暂不严格区分亚型,使用“植物源外泌体样纳米囊泡”作为统称,更为审慎。 |
标志物 | 依赖CD9、CD63、CD81、TSG101等经过验证的特异性蛋白标志物进行鉴定和质控。 | 明确承认缺乏公认的特异性蛋白标志物。不强制检测特定蛋白,建议采用形貌、粒径、总蛋白/RNA含量等通用表征手段进行综合鉴定。 |
分离纯化 | 超速离心法是经典方法;免疫亲和捕获法因有特异性抗体,是重要的纯化手段。
| 指出植物原料中的纤维素、淀粉等高分子量成分可能导致离心困难。因缺乏公认标志物,免疫亲和捕获法不作为通用方法,主要依赖差速离心、尺寸排阻色谱等物理分离方法。 |
质量控制 | 重点关注颗粒浓度、粒径分布、特定标志物阳性表达、杂质限量等。
| 除基本物理指标外,特别强调控制植物次生代谢产物、色素等植物源性杂质。对于特定植物来源(如油橄榄叶),还会将标志性活性成分(如羟基酪醇)的含量纳入质控。 |
应用导向 | 侧重于疾病诊断标志物、药物递送系统等医药领域。 | 适用范围明确覆盖药品、保健食品、化妆品、功能饮料等,更贴近植物资源的传统应用领域。 |
标准化程度
| 有ISEV的MISEV指南、ISO/TC276系列标准等相对成熟的国际共识和标准体系。
| 属于新兴领域,标准化工作刚刚起步。尽管有《油橄榄叶来源的纳米囊泡》等针对单一植物的团体标准出现,但跨物种的通用标准仍在建立中,本标准的制定具有前瞻性。 |
核心差异总结与建议。简单来说,在制定的标准与国际现有标准最主要的区别在于“不确定性”和“特殊性”的处理上。面对“不确定性”:在植物源外泌体许多基础科学问题(如精确分类、特异标志物)尚未完全解决的情况下,您的标准采取了务实和开放的态度,强调通用表征和功能验证,而非套用可能不适用的动物模型。应对“特殊性”:标准充分考虑了植物原材料处理、杂质控制以及多行业应用等特殊要求,这使得标准更具可操作性和产业指导价值。
基于以上分析,为了使标准更具国际视野和引领性,可以考虑:在标准中适当关注或引用国内最新的相关团体标准(如T/CIET 1686-2025《植物源性细胞外囊泡分离纯化工艺技术规范》),以体现与国内最新进展的对接。随着研究深入,未来可适时引入关于植物源外泌体生物活性(如抗炎、促进修复)的功能性评价方法作为补充质控手段。
正在制定的《植物源外泌体样纳米囊泡某标准》与ISO/TC276框架下的通用生物技术标准,在技术侧重上存在系统性的差异。这些差异主要源于标准类型、适用对象和具体技术目标的根本不同。
比较维度 | 该某标准 (PELNVs专用)
| ISO/TC276 相关标准 (通用生物技术框架) | 差异本质
|
标准类型与范围 | 产品/技术标准:针对特定产品(PELNVs)的制备、鉴定、质量控制和应用。 | 基础通用标准:为生物技术领域(如术语、样本库、数据管理)提供通用框架和原则。 | 专用性 vs. 通用性
|
核心适用对象 | 植物源外泌体样纳米囊泡(PELNVs)本身。 | 广泛的生物资源(微生物、细胞、生物样本等)及相关数据。 | 对象特定 vs. 对象广泛 |
技术内容焦点
| 全过程技术规范:详细规定从原料处理、分离纯化(如差速离心、超滤)到性状(粒径、标志物)、纯度、安全性等具体指标。 | 体系与质量管理:侧重于生物资源中心的数据管理规范、生物样本库的通用能力要求等宏观管理体系和流程。
| 技术操作细节 vs. 体系管理框架
|
术语与定义
| 需定义PELNVs等特定术语,并处理其特殊性(如植物特异性标志物尚不明确)。 | 提供基础性的术语和定义,旨在统一不同国家和领域的基本概念。 | 解决特殊性问题 vs. 建立基础共识 |
制备与鉴定
| 重点关注适用于植物基质的制备方法(如处理纤维素、淀粉等杂质)和鉴定手段(如电镜、NTA)。 | 不涉及具体产品的制备工艺,可能涵盖生物样本库操作或生物分析方法的通用要求。
| 针对材料特性 vs. 方法学通用性
|
核心差异详解。基于上表的对比,我们可以更深入地理解这些差异背后的逻辑:专用性与通用性的互补关系。该标准与ISO/TC276标准并非“竞争”或“矛盾”关系,而是互补的。该标准填补了ISO通用框架在植物源纳米囊泡这一具体细分领域的技术空白。可以将ISO标准视为构建行业标准体系的“地基和骨架”,而该标准则是在此基础上为PELNVs这个“房间”进行的“精装修”。在进行国际交流或申报时,遵循ISO的基础原则(如质量管理、数据规范)能增强您标准的严谨性和国际认可度。

技术细节与体系管理的不同层面。ISO/TC276标准(如ISO 20387生物样本库标准)关注的是一个机构或平台是否具备可靠保存和提供生物资源的能力。而该标准直接指导如何生产出一个质量可控的PELNVs产品。例如,该标准需要详细规定超速离心的转速时间、蔗糖密度梯度的浓度范围、纳米颗粒跟踪分析(NTA)的校准标准等,这些具体技术参数在管理体系标准中是不会涉及的。

应对PELNVs的特殊挑战。这标准必须解决一些ISO通用标准无法覆盖的特殊技术难题,这恰恰是其价值所在:标志物问题:动物细胞外泌体有CD9、CD63等相对公认的标志物,而PELNVs目前缺乏这类特异性标志物。该标准可能更强调通过物理化学性质(粒径、形态)和功能活性等多指标进行综合鉴定,而非依赖单一的蛋白标志物。制备工艺特殊性:植物原料中大量的纤维素、淀粉等成分会给离心和纯化带来困难,您的标准需要针对这些植物特有的杂质提出有效的解决方案。
总结与建议。简单来说该某标准与ISO/TC276标准的主要差异在于:该某标准是深入PELNVs领域的技术“操作手册”,而ISO/TC276标准是构建整个生物技术领域的“通用语言”和“管理宪法”。在制定该某标准时,一个很好的思路是:在原则性、框架性条款上参考和遵循ISO的基础标准,以确保科学性;同时,将主要精力和技术创新点放在解决PELNVs特有的技术挑战和应用需求上。

PELNVs领域当前的竞争主要集中在几个关键维度。技术壁垒的构建:核心在于能否建立稳定、高效、可规模化的PELNVs制备工艺。安龄生物等公司正致力于解决大规模生产中的技术难点,而诺斯贝尔推出的“PhytoExo™ PLUS+ 植物愈伤细胞外泌体递送技术”则代表了在功效成分靶向递送这一细分技术上的深化。法规与标准的抢占:这是一个至关重要的竞争维度。由于国内尚未建立PELNVs生产、临床和质量控制的统一标准,谁能更深入地参与并影响未来标准的制定,谁就能在市场竞争中占据有利位置。《中草药囊泡研究与应用专家共识(2023年版)》的发布,正是为了推动建立行业规范,未来标准至关重要。总体来看,PELNVs领域的竞争是一场技术、资源、战略眼光和耐心的综合比拼。目前尚未形成稳定的市场格局,真正的竞争或许才刚刚开始。



