

7月30日,上海市委副书记、市长龚正主持召开市政府常务会议,要求按照市委部署,促进高端医疗器械产业全链条发展。会议原则同意《上海市促进高端医疗器械产业全链条发展行动方案》并指出,高端医疗器械迭代升级速度日益加快,要放大创新策源的研发优势,聚焦重点产品方向,集中力量攻坚,力争取得标志性成果。要持续推进“研发+临床+制造+应用”全链条加速,推动审评审批再提速,支持创新器械产品入院、进店、上网、下社区。要加快建设产业集聚区,支持本地创新型企业做大做强,培育具有国际竞争力的龙头企业,推动沪产创新器械走向全球。

我谈谈自己的看法。《北京市医疗器械产业提质升级行动计划(2024-2026年)》京经信发〔2024〕60号(简称《行动计划》)于2024年11月发布。《行动计划》是为了贯彻落实《北京市加快医药健康协同创新行动计划(2024-2026年)》,紧抓高端医疗器械创新发展新机遇,以打造国家级高端创新医疗器械产业集群为主要抓手,促进北京市医疗器械产业实现创新链融通、产业链整合、价值链提升,加快迈入新发展阶段,制定的行动计划。《行动计划》以临床需求为导向、以技术融合创新为引领、以促进医产学研协作为抓手、以强化区域协同支撑为总体思路,提出到2026年总体规模突破500亿元、打造专业化产业园区5个以上、创新品种超100个,培育亿元级新产品10个以上,吸引5家以上全球医疗器械龙头企业,涌现一批专精特新企业;新增一批创新载体,优化市场生等具体目标,力争到“十五五”末建成对标世界一流水平的高端创新医疗器械产业集群。
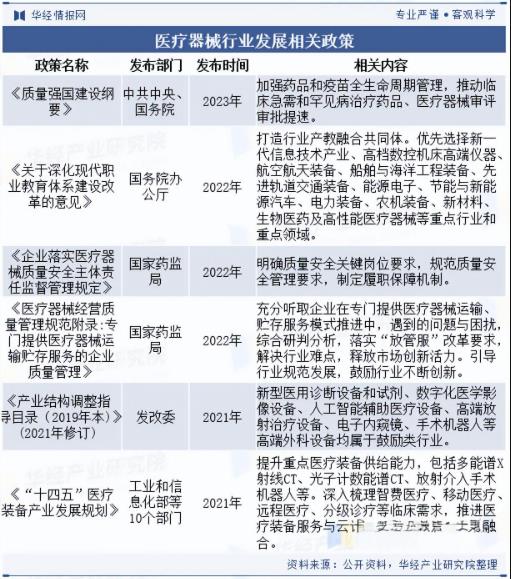
《行动计划》提出,北京将实施“数智引擎升维工程”,推动医疗大模型构建、迭代和应用,加快医学影像等医疗健康大数据合规流通;实施“企业培优倍增工程”,通过建设企业技术中心、产业创新中心等载体,推进数智化、绿色化转型及产业资源整合,促进企业“梯度化”成长;鼓励医疗机构参与“医工融合示范工程”,打造示范应用和培训中心,建立协作创新体系;“产业生态创优工程”将以专业化园区建设为载体,谋划覆盖研发、中试、临床的第三方综合服务平台,打造全链条服务体系。从产业链、供应链的角度上看,医疗器械上下游仍面临关键“卡点”“难点”。为此《行动计划》专门提出区域协同补链工程,开展京津冀联合招商,构建产业链、供应链生态圈。上海没有反应。
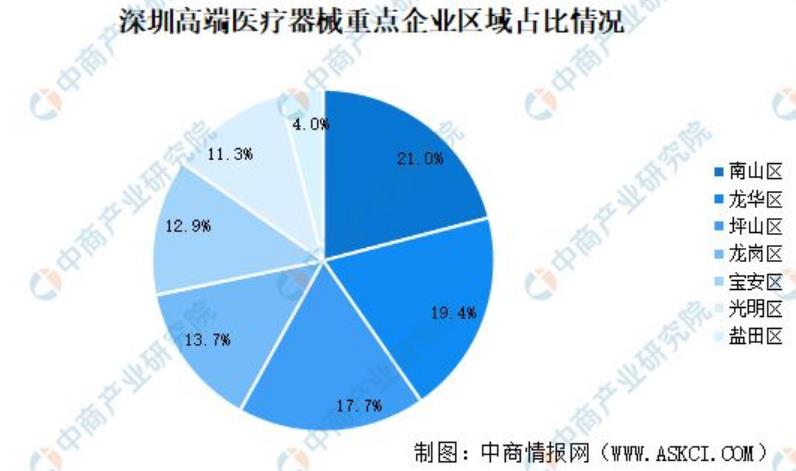
2025年4月深圳市发展和改革委员会 深圳市卫生健康委员会 深圳市市场监督管理局 深圳市医疗保障局关于印发《深圳市全链条支持医药和医疗器械发展若干措施》的通知。9个方面32条,6月份地方政府解读政策亮点为1.落实国家和省新要求。聚焦临床前研究、临床试验、注册审批、生产制造、入院推广等医药和医疗器械产业发展全链条环节,提出具体政策措施,落实国家、省关于创新药械全链条支持的工作要求。2.覆盖新技术新赛道新业态。对近年来涌现的“人工智能+”药械、生物制造、细胞与基因治疗、宠物药械、罕见病药、中医药、药械产品出海等新技术新赛道新业态,提出专项全链条支持举措。3.支持标准体现新力度。围绕“人工智能+”药械、宠物药、药械产品出海等方面,在产品研发到入院具有里程碑意义的节点上,给予“人无我有、人有我优”的政策支持力度。4.支持方式体现新温度。政策支持方式持续优化,对取得1类创新药上市批件的企业直接给予奖励,不再核算研发费用,有效避免政策申报程序繁琐,简化的申报流程让企业享受到更多便捷。

上海有些急了。这次出台的《上海市促进高端医疗器械产业全链条发展行动方案》把聚焦重点产品方向,力争取得标志性成果放在首位,需要一炮打响。我认为上海将通过“技术攻坚×临床赋能×政策护航”三维协同模式,聚焦重点产品方向实现标志性突破。核心技术攻坚:锁定三大前沿领域。1.高端医学影像设备。超高端影像系统:集中攻关光子计数CT、7T超高场磁共振(联影医疗研发中的全球首台光子计数CT)、全景动态PET-CT(联影2米PET-CT已实现全身扫描30秒完成)。国产化目标:突破CT球管、高分辨率探测器等核心部件,目标国产化率超60%。2.手术机器人及智能器械。微创手术机器人:支持微创机器人四臂腔镜手术机器人产业化(国内首个获批产品,打破国外垄断);推动神经介入手术机器人精度达亚毫米级(天智航骨科机器人已积累超11万例手术)。AI辅助诊断:开发冠脉AI诊断软件,支持开立医疗4K超声内镜进入创新器械绿色通道。3.先进治疗设备。质子治疗系统:推动艾普强粒子国产质子治疗系统规模化应用(国内首个获批,性能达国际先进水平),降低肿瘤治疗成本30%。精准放疗设备:研发小型化重离子治疗装置,实现国产替代。

全链条赋能:打通“研发→临床→制造→应用”堵点。1.研发端:强化协同攻关平台。产学研医一体:建设上海市高端医疗装备创新中心(杨浦区),支持企业联合高校共建CMDO平台(如昊丰医疗与上理工合作实现神经介入器械全线国产化)。揭榜挂帅机制:设立专项基金支持“卡脖子”技术(如ECMO中空纤维膜),单个项目最高支持3000万元。2.临床端:加速转化与验证。研究型医院建设:允许三甲医院按10%床位设置研究型病房,缩短临床试验启动时间至25周内(原平均40周)。真实世界数据应用:开放106万人队列数据库,允许AI器械以真实世界证据替代40%传统临床试验。3.制造端:智能化与绿色升级。工业级智能体应用:推广“AI+制造”柔性产线(如联影东南亚分装中心降本20%),关键工序自动化率要求超90%。绿色制造标准:强制披露碳足迹,推广聚乳酸导管等生物基材料。4.应用端:强制准入与支付保障。创新产品“应配尽配”:要求三级医院1个月内配备纳入“新优药械”目录的产品(如DRG/DIP改革中单列支付)。社区下沉目标:便携超声、AI诊断助手覆盖90%社区卫生中心,新增60类耗材纳入社区医保。

政策护航:资源倾斜与国际化突破。1.审评审批再提速。优先审批程序:二类器械审评压缩至40个工作日,创新产品享“专班制”服务(专人全程跟踪)。电子化与AI审评:推行eRPS电子申报系统,AI自动核验资料错误率降40%;区块链存证保障监管可追溯。2.出海与国际认证。千万元级认证支持:对通过FDA/CE认证企业给予最高1000万元奖励(如联影医疗覆盖50国,海外收入目标占比25%)。“一带一路”布局:援建项目优先采购上海装备,在东南亚建海外仓降物流成本20%。3.金融与人才保障。千亿产业基金:生物医药母基金定向投资脑机接口、3D打印植入物等前沿领域。医工复合型人才:高校增设医疗器械工程硕士点,推行“企业导师制”(复旦、交大试点)。

上海高端医疗器械重点攻关方向与目标。
领域 | 标志性产品 | 技术目标 | 产业化目标 |
医学影像
| 光子计数CT、7T磁共振 | 空间分辨率≤0.1mm,扫描速度提升50% | 2027年国产市占率超40% |
手术机器人
| 四臂腔镜机器人、骨科导航系统 | 操作精度≤0.1mm,力反馈延迟≤10ms | 累计手术量突破50万例 |
先进治疗设备
| 质子治疗系统、小型化重离子设备 | 肿瘤定位误差≤1mm,治疗效率提升30% | 单台治疗成本降至进口设备60% |

上海模式的突破点。上海将通过 “聚焦赛道×全链协同×生态赋能” 实现标志性成果:技术端:以“揭榜挂帅”攻坚光子CT、手术机器人等“国之重器”,配套千万元级研发支持;临床端:以研究型医院+真实世界数据缩短转化周期,压缩伦理审查至3周内;市场端:以“应配尽配”政策强制入院,结合千亿基金+出海认证推动国产替代与全球化。最终构建 “研发—临床—制造—出海”闭环生态,助力国产高端器械从“技术跟跑”转向“全球领跑”。

其中要持续推进“研发+临床+制造+应用”全链条加速。产业全链条发展是指通过系统化整合“研发—临床—制造—应用”四大核心环节,打通技术转化与市场落地的堵点,实现产业链各节点的协同升级。理论框架:全链条发展的核心逻辑。环节定义与价值分布。研发端:聚焦核心技术突破(如AI算法、精密传感器),是产业高附加值环节(毛利率超50%)。临床端:衔接技术验证与产品转化,依赖研究型医院和真实世界数据(RWD),耗时占全周期40%。制造端:通过智能化生产(如工业级智能体)降本增效,关键工序自动化率需达90%以上。应用端:覆盖市场准入(入院、出海)与用户反馈,国产器械在三甲医院渗透率不足30%是核心痛点。

2.协同效应模型。技术流:研发输出→临床验证→制造工艺优化→应用场景迭代(如济南国科医工激光技术从实验室到手术室仅2年)。数据流:临床需求反馈→研发方向调整→制造参数校准(如AI医疗器械通过临床数据优化算法)。政策流:审评审批提速→采购政策倾斜→国际标准对接(如国家药监局十项举措缩短创新产品上市周期30%)。关键瓶颈:全链条断点分析。1.研发与临床脱节。高校科研成果转化率不足15%,主因医工交叉机制缺失(如医生创意难对接企业资源)。真实世界数据应用滞后,AI诊断算法仅20%采用RWD替代传统试验。2.制造环节韧性不足。核心部件“卡脖子”(如CT球管国产化率40%),供应链备份覆盖率低于50%。绿色制造标准缺位,生物基材料渗透率不足10%。3.应用端准入壁垒。三级医院采购外资设备占比超70%,国产替代政策执行率待提升。出海认证周期长,企业获欧盟MDR认证平均需18个月,较国际巨头多6个月。

政策实践:国内外全链条加速案例。1.国内政策创新。上海模式:研发端:设立50亿专项基金支持“揭榜挂帅”(如ECMO膜技术攻关)。临床端:浦东新区压缩临床试验立项至1个月(行业平均3个月),创新械品100%入院。制造端:临港新片区建设高端影像制造基地,配套跨境物流降本20%。应用端:推动便携超声覆盖90%社区,CE认证辅导团队助力50家企业出海。国家药监局十项举措:创新特别审查程序前置至研发阶段,AI医疗器械变更注册简化。加速制定脑机接口电极、医用外骨骼机器人等国际标准。2.国际经验借鉴。美国FDA“突破性设备计划”:通过“附条件批准”机制,使创新型器械上市周期缩短40%(如神经介入机器人)。欧盟MDR协同认证:建立跨国互认实验室,企业一地认证即可通行27国。

企业实践:全链条协同标杆
企业案例 | 研发端突破 | 制造端升级 | 应用端拓展 |
沛嘉医疗
| 全球首创TAVR抗反流瓣膜(TaurusTrio) | 苏州工业园智能产线,良品率99% | 神经介入产品市占率25%,欧美同情救治13例 |
济南国科医工
| 激光光谱技术(血培养时间从48h→9h) | 中试平台千万元级成果转化 | 甲状旁腺检测仪三甲医院覆盖率60% |
联影医疗 | 光子计数CT国产化
| 东南亚分装中心降本20% | uInterv C550手术机器人获三类证 |

未来路径:全链条优化策略。1.环节强化。研发端:建立“临床需求库”(如川渝领先用户社区),医工交叉项目占比提升至30%。制造端:推广“工业互联网+5G”柔性产线,核心部件备份供应商增至3家。2.政策深化。扩大“附条件批准”范围,对脑机接口、AI医疗软件开放绿色通道。将国产采购比例纳入医院评级指标,社区医疗强制配置国产设备。3.全球化布局。共建“一带一路”海外仓(如联影东南亚中心),本地化分装降低关税成本。主导ISO/TC 215医疗信息标准制定,推动国产标准国际化。

挑战与趋势。技术伦理挑战:AI医疗算法的数据隐私风险需通过联邦学习技术破解。产业集中化:预计2030年长三角、珠三角集群产值占全国60%,中西部需差异化布局(如湖南聚焦康复机器人)。新质生产力方向:医用机器人、基因编辑器械、量子成像设备将成为全链条竞争新高地。产业全链条发展的本质是 “技术-资本-政策”三链融合:技术攻坚需以临床需求为原点(如春雨行动的医生创意转化);资本赋能需覆盖早期研发(千亿产业基金)到出海拓展(跨境金融);政策设计需贯穿全生命周期(从创新审查到国际标准)。唯有打破环节割裂,才能实现国产高端器械从“替代进口”到“全球定义”的跃迁。

上海通过系统性制度创新与全链条资源整合,显著加速创新医疗器械审评审批流程,并打通“入院、进店、上网、下社区”的市场准入堵点,具体措施如下:审评审批制度改革:全周期提速。1.注册前置服务与流程优化。提质增效2.0行动:实施《医疗器械审评审批提质增效扩能行动方案(2023-2024)》,将二类器械注册周期压缩至100天(较2020年提速33%),审评用时缩短至34个工作日。创新产品“专班制”:对创新器械、揭榜挂帅项目提供“提前介入+全程跟踪”服务,建立12家生物医药注册指导服务站,2021-2023年推动81个三类器械进入国家创新绿色通道(获批34张注册证,全国第二)。分类快速审评:简化AI算法优化类产品变更注册流程,探索电子说明书应用;对人工智能医疗器械、手术机器人等动态调整管理类别,缩短技术迭代周期。
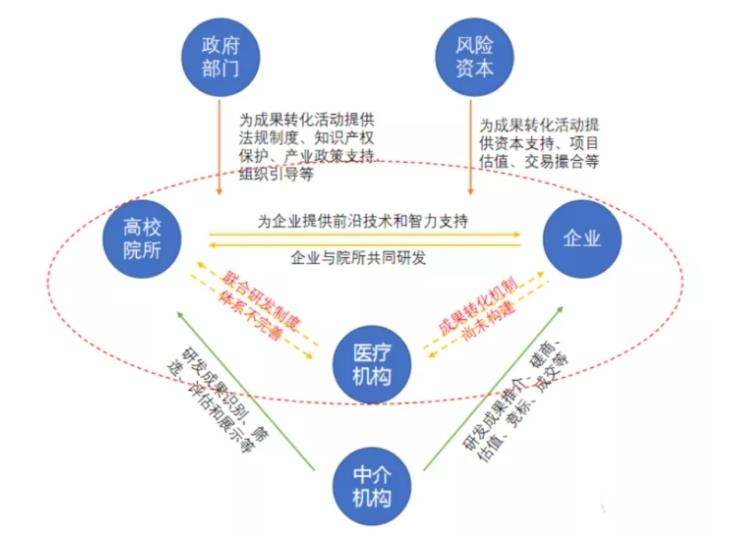
2.检验检测技术赋能。上海医械院创新机制:建立“无源器械创新服务机制”,为动脉瘤封堵装置等产品开辟检测“绿色通道”,周期缩短33%。搭建人工心脏瓣膜流场测试平台(国内首个),牵头制定DPIV技术标准,助力5家企业快速获国内外注册批准。呼吸麻醉设备重点实验室:开发呼吸机自动化测试系统,填补国内空白,检测效率提升40%。加速市场准入:打通“院-店-网-区”。1.创新器械“入院”强制配备。医保目录联动:创新器械纳入国家医保目录或上海“新优药械”目录后,医疗机构需在1个月内按“应配尽配”原则配备,不得以药占比、预算限制为由拒用。支付倾斜政策:DRG/DIP改革中对创新器械诊疗项目单列支付,提高支付标准且不受高倍率病例限制。国家医保谈判器械前三年实行医保预算单列(如CAR-T疗法),缓解医院成本压力。

2.多渠道“进店+上网”覆盖。药店渠道拓展:700余家定点药店接入医保电子处方平台,支持创新器械销售;取消器械本地医保编码,全面使用国家编码简化结算流程。药店设“智能健康站”,提供CGM、呼吸机等体验服务(如鱼跃、微创合作项目)。线上平台整合:“随申办”上线“保险码”板块,支持38款商保产品购买;“一码通赔”平台实现10家保险公司快速理赔,提升器械可及性。3.社区健康“下沉”行动。设备覆盖目标:推动便携超声、AI诊断助手覆盖90%社区卫生中心,2024年新增60类新型耗材纳入社区医保支付(如慢病管理设备)。数据赋能基层:建立社区健康数据库,支持AI辅助诊断系统优化筛查效率(如无创血糖仪误差<5%)。
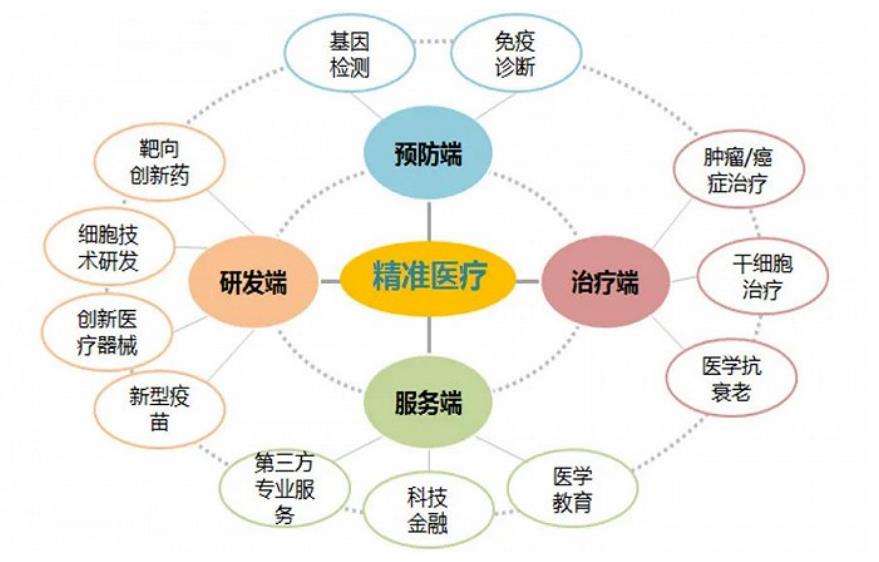
监管与产业协同:构建创新生态。1.真实世界数据应用。建立医学队列数据库(覆盖106万份样本),开放共享临床数据,允许AI医疗器械以真实世界证据替代40%传统临床试验。2.医保-商保联动机制。沪惠保扩容:2024版覆盖41种特药,将“新优药械”全部纳入,参保超600万人;医保大数据实验室支持8款商保产品开发,提升支付能力。企业税收激励:全国首创企业为员工购买商业健康险的所得税抵扣细则,激发采购需求。
跨境便利化与国际对接。1.研发物品通关优化。拓展研发用物品“白名单”(含微量检测标准品),免办农业、环保进口许可证,通关效率提升60%。2.国际认证与出海支持。临港新片区设MDR/CE专项辅导团队,目标2026年前助50家企业获欧盟认证;联影医疗在东南亚建分装中心,物流成本降低20%。国家药监局推动全球监管协调,简化出口销售证明,支持企业主导ISO医用机器人等国际标准制定(如外骨骼机器人标准)。

核心突破。上海通过 “制度创新(审评提速×强制入院)+技术赋能(检测自动化×AI数据应用)+支付改革(医保商保联动)” 三维协同,实现:审评端:注册周期压缩1/3,创新产品优先准入;市场端:社区覆盖率达90%,药店/线上全渠道打通;国际端:跨境通关与认证效率双提升。最终形成 “快审批-强准入-广覆盖” 的创新器械全链条支持体系,为国产高端器械替代进口与全球化竞争提供核心引擎 。

加快建设产业集聚区,支持本地创新型企业做大做强,培育具有国际竞争力的龙头企业。上海可以通过“空间集聚×政策赋能×生态协同”三维策略,系统性建设医疗器械产业集聚区,并加速培育具有国际竞争力的龙头企业。产业集聚区布局与功能定位。1.“三区联动”空间规划。闵行北部集聚区:分设枢纽片区(南虹桥)、前湾片区(华漕镇)、医学园区三大功能区,依托新虹桥国际医学中心、临港浦江国际科技城等平台,整合“研发-生产-应用”全链条资源。重点发展高端影像设备、体外诊断试剂,打造长三角医疗器械创新高地。
嘉定“械谷”:以瑞金医院国家医学中心为核心,构建“一核一岛”空间布局(研发平台+生产制造),聚焦手术机器人、脑机接口等创新器械。徐汇AI赋能集群:全国首个“AI+仪器仪表产业集聚区”,以自仪院为核心,布局智能传感器、医疗检测装备研发,推动AI与高端器械深度融合。2.专业化平台支撑。临床转化平台:瑞金医院国家医学中心联动“械谷”创新中心,加速医工结合成果转化(如手术机器人临床验证周期缩短40%)。共性技术平台:嘉定虹桥国际创新医疗器械产业园提供研发评价、联合攻关服务,助力企业突破核心部件“卡脖子”问题(如CT球管国产化)。
全链条政策支持体系。1.研发与审批提速。优先审评通道:二类器械注册周期压缩至40个工作日,AI辅助审评系统自动核验资料,错误率下降40%。揭榜挂帅机制:设立50亿元专项基金,支持企业攻克ECMO膜技术等关键领域,单个项目最高资助3000万元。2.市场准入与支付保障。创新产品“应配尽配”:国家医保目录或上海“新优药械”产品发布1个月内,医疗机构必须配备使用,DRG/DIP改革中单列支付。社区下沉强制覆盖:便携超声、AI诊断设备覆盖90%社区卫生中心,60类新型耗材纳入社区医保支付。3.国际化认证支持。出海专项辅导:临港新片区设MDR/CE认证团队,AI模拟欧盟审评流程,企业认证通过率提升35%。千万元级奖励:对通过FDA/CE认证企业给予最高1000万元资金支持(如联影医疗海外收入目标占比25%)。

创新型企业培育路径。1.分层培育龙头企业。技术攻坚型:支持联影医疗研发光子计数CT、微创机器人推进四臂腔镜手术机器人产业化,打破国际垄断。场景整合型:上海医药依托渠道优势,主导社区医疗设备下沉与智慧养老方案落地。出海先锋型:推动天智航骨科机器人(手术超11万例)通过FDA认证,开拓欧美市场。2.产学研医协同机制。临床需求驱动:三甲医院按10%床位设研究型病房,开放106万人队列数据库,允许AI器械以真实世界数据替代40%传统试验。高校联合实验室:上海交大、华东理工等共建“智能传感创新研究中心”,攻关医用高精度传感器。
国际化生态构建。1.全球资源整合。海外研发中心:支持企业在欧美设立分支机构,组建跨国研发团队(如联影东南亚分装中心降本20%)。国际多中心试验:与“一带一路”国家共建临床试验基地,推进数据互认,缩短海外上市周期。2.跨境服务优化。通关便利化:研发用物品“白名单”免办进口许可,特殊物品联合监管机制支持细胞治疗产品快速通关。商事争议解决:推动上海成为国际商事争议优选地,法律、专利服务机构全球化布局。
金融与要素保障。1.千亿级基金赋能。产业母基金:生物医药基金定向投资脑机接口、3D打印植入物等前沿领域,培育新质生产力。CVC并购基金:国资基金联合企业组建风险投资基金,支持海外并购(如10亿元“AI+仪器仪表”基金投早投小)。2.数据要素开放。医保数据实验室:开放真实世界医保数据,助力企业研发与商保产品开发(已支撑8款商保产品)。跨境数据流动试点:临港新片区探索生物医药数据安全跨境流动,加速全球协作。

上海模式的核心突破。上海通过 “空间集聚(三区联动)×政策闭环(研发到出海)×生态赋能(人才-数据-资本)” 策略:集聚区建设:闵行、嘉定、徐汇差异化布局,形成千亿级产业集群;企业培育:分层支持联影、微创等龙头技术攻坚与国际化,目标2027年培育2-3家海外收入超百亿企业;制度创新:从“应配尽配”强制入院到AI审评提速,打通全链条堵点,推动国产器械从“替代进口”到“定义全球标准”。



